重磅!乙肝患者迎来曙光!全球首款功能性治愈药GSK836(bepirovirsen)将于2026年上市,部分患者实现停药无复发
据葛兰素史克(GSK)官网公布的2024年财报,全球首个乙肝功能性治愈药GSK3228836(bepirovirsen)上市时间敲定为2026年,已公布临床试验研究数据显示可实现30%患者停药后无复发。
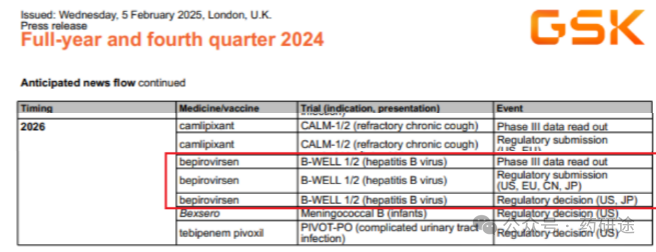
从公司年报公布的GSK3228836(bepirovirsen)上市注册申请计划是2026年优先在美国、中国、欧洲、日本递交上市申请(NDA),预计2026年可获得美国、日本的官方审批决定(见上图GSK2024年财报截图红色框内容),也就是可能先在美国和日本获得监管机构的批准上市许可。
GSK3228836(bepirovirsen)的研发里程碑
早期研发与合作:2019年,葛兰素史克从Ionis Pharmaceuticals获得了Bepirovirsen的许可,支付了2500万美元的预付款。
突破性疗法认定:2021年,Bepirovirsen获得了中国药品审评中心的突破性疗法认证。
快速通道资格:2024年,Bepirovirsen获得了日本厚生劳动省的“SENKU(先驱)指定”以及美国FDA授予的“Fast track”(快速通道)资格。
GSK3228836(bepirovirsen)的临床试验进展
B-Well 1和B-Well 2试验:这两项III期试验均于2023年第一季度启动,旨在确认Bepirovirsen在慢性乙型肝炎患者中的疗效和安全性,目前处于“Active,not recruiting”状态。
B-United试验:这是一项IIb期多中心、随机、部分安慰剂对照、双盲临床试验,于2024年第四季度启动,旨在评估Daplusiran/Tomligisiran序贯Bepirovirsen治疗在接受核苷(酸)类似物背景治疗的慢性乙型肝炎患者中的安全性和有效性。2024年11月20日,该试验获得中国国家药品监督管理局药品审评中心批准临床。
目前还在开展的相关联合治疗慢乙肝的临床试验研究
B-United试验:一项正在进行的二期临床试验,研究bepirovirsen与daplusiran/tomligisiran序贯治疗的效果。
B-CLEAR试验:一项二期临床试验,研究病毒载量抑制患者的基因型、疾病异质性与治疗反应之间的关联。
在2026年提交监管申请之前,GSK预计将在2025年的亚太肝病学会年会、欧洲肝病学会年会和美国肝病学会年会上公布部分临床数据。
GSK3228836(bepirovirsen)递交上市申请计划
优先开发与目标时间:
据Fierce报道,葛兰素史克(GSK)CEO Emma Walmsley在2024年第四季度和全年财报电话会议中表示,公司优先开发可功能性治愈慢乙肝药物GSK3228836(bepirovirsen),并计划在2026年获得监管机构对慢性乙型肝炎治疗的批准决定。
向监管申请提交: GSK计划在2026年在美国、欧洲、中国和日本提交GSK3228836(bepirovirsen)的监管申请。此前,该药物已在中国、美国和日本获得“突破性药物程序认定”、“快速审评审批通道”和“SENKU(原名SAKIGAKE)指定”,这意味着在这些国家的上市审批会得到优先处理 。
此外,据悉GSK在中国招聘负责该重磅乙肝产品的医学联络官,也表明其上市准备工作正在推进。
GSK3228836(bepirovirsen)的其它相关信息详看:有望功能性治愈乙肝的在研药物Bepirovisen | 已获得FDA快速通道审评资格
参考文献:
[1]GSK官网
[2]Fierce官网
本文中涉及的信息仅供参考,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。若您想了解具体疾病诊疗信息,请遵从医生或其他医疗卫生专业人士的意见或指导。
下一篇:多款停售!美系车企遭反噬!
